Jak działają i działają baterie
 W najszerszym tego słowa znaczeniu w technice termin „bateria” odnosi się do urządzenia, które pozwala w pewnych warunkach pracy gromadzić określony rodzaj energii, aw innych wykorzystywać ją na potrzeby człowieka.
W najszerszym tego słowa znaczeniu w technice termin „bateria” odnosi się do urządzenia, które pozwala w pewnych warunkach pracy gromadzić określony rodzaj energii, aw innych wykorzystywać ją na potrzeby człowieka.
Stosuje się je tam, gdzie konieczne jest gromadzenie energii przez określony czas, a następnie wykorzystanie jej do przeprowadzenia dużych pracochłonnych procesów. Na przykład akumulatory hydrauliczne stosowane w śluzach pozwalają statkom wznieść się na nowy poziom w korycie rzeki.
Baterie elektryczne działają z elektrycznością na tej samej zasadzie: najpierw gromadzą (akumulują) energię elektryczną z zewnętrznego źródła ładowania, a następnie przekazują ją podłączonym odbiorcom do pracy. Ze swej natury należą do źródeł prądu chemicznego zdolnych do wykonywania okresowych cykli wielokrotnego rozładowania i ładowania.
Podczas pracy stale zachodzą reakcje chemiczne między składnikami płytek elektrod z ich substancją wypełniającą - elektrolitem.
Schemat ideowy urządzenia bateryjnego można przedstawić za pomocą uproszczonego rysunku, gdy dwie płytki z różnych metali z drutami są włożone do korpusu naczynia, aby zapewnić styki elektryczne. Między płytki wlewa się elektrolit.
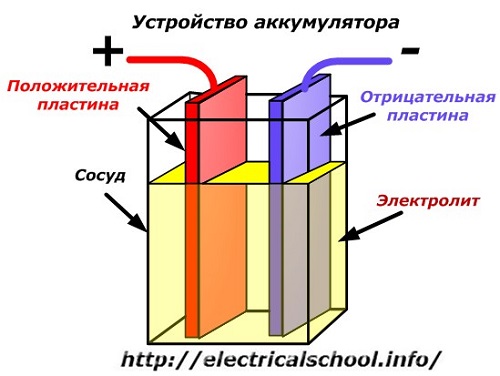
Działanie baterii po rozładowaniu
Kiedy obciążenie, takie jak żarówka, jest podłączone do elektrod, tworzony jest zamknięty obwód elektryczny, przez który przepływa prąd rozładowania. Powstaje w wyniku ruchu elektronów w częściach metalowych i anionów z kationami w elektrolicie.
Proces ten jest konwencjonalnie pokazany na schemacie z konstrukcją elektrody niklowo-kadmowej.
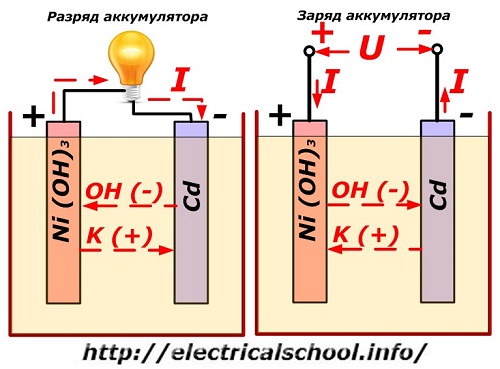
Tutaj jako materiał elektrody dodatniej zastosowano tlenki niklu z dodatkami grafitu, które zwiększają przewodność elektryczną. Metalem elektrody ujemnej jest gąbczasty kadm.
Podczas rozładowania cząsteczki aktywnego tlenu z tlenków niklu są uwalniane do elektrolitu i kierowane na płyty ujemne, gdzie następuje utlenienie kadmu.
Wydajność baterii podczas ładowania
Gdy obciążenie jest wyłączone, na zaciski płytki przykładane jest stałe (w niektórych sytuacjach pulsujące) napięcie o wartości większej niż napięcie naładowanego akumulatora o tej samej biegunowości, gdy zaciski dodatnie i ujemne źródła i odbiornika pokrywają się .
Ładowarka zawsze ma większą moc, co „tłumi” energię resztkową w akumulatorze i wytwarza prąd elektryczny w kierunku przeciwnym do rozładowania. W rezultacie zmieniają się wewnętrzne procesy chemiczne między elektrodami a elektrolitem. Na przykład na pudełku płytek niklowo-kadmowych elektroda dodatnia jest wzbogacana tlenem, a ujemna - do stanu czystego kadmu.
Gdy akumulator jest rozładowywany i ładowany, zmienia się skład chemiczny materiału płytek (elektrod), ale elektrolit się nie zmienia.
Metody podłączenia baterii
Połączenie równoległe
To, jaki prąd wyładowania może wytrzymać dana osoba, zależy od wielu czynników, ale przede wszystkim od konstrukcji, użytych materiałów i ich wymiarów. Im większa powierzchnia płytek przy elektrodach, tym większy prąd mogą wytrzymać.
Zasada ta służy do łączenia ogniw tego samego typu równolegle w akumulatorach, gdy konieczne jest zwiększenie prądu do obciążenia.Ale aby naładować taką konstrukcję, konieczne będzie zwiększenie mocy źródła. Ta metoda jest rzadko stosowana w przypadku gotowych konstrukcji, ponieważ teraz znacznie łatwiej jest od razu kupić niezbędną baterię. Ale używają go producenci akumulatorów kwasowych, łącząc różne płyty w pojedyncze bloki.
Połączenie szeregowe
W zależności od użytych materiałów, między dwiema płytami elektrodowymi akumulatorów, które są powszechnie stosowane w życiu codziennym, można wytworzyć napięcie 1,2 / 1,5 lub 2,0 V. (W rzeczywistości ten zakres jest znacznie szerszy.) Oczywiście nie jest wystarczający dla wielu urządzeń elektrycznych. Dlatego akumulatory tego samego typu są łączone szeregowo i często odbywa się to w jednym przypadku.
Przykładem takiego projektu jest szeroko rozpowszechniony rozwój motoryzacji oparty na kwasie siarkowym i ołowianych płytach elektrodowych.
Zwykle wśród ludzi, zwłaszcza wśród kierowców transportu, zwyczajowo nazywa się każde urządzenie baterią, niezależnie od liczby jego elementów składowych - skrzynek. Jednak nie jest to całkowicie poprawne.Konstrukcja, złożona z kilku połączonych szeregowo pudełek, jest już baterią, na której umieszczono skróconą nazwę «АКБ»... Jej wewnętrzną strukturę pokazano na rysunku.
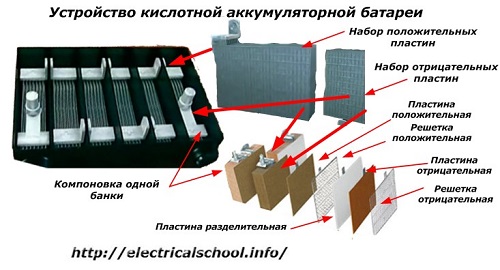
Każdy ze słoiczków składa się z dwóch bloków z kompletem płytek na elektrodę dodatnią i ujemną. Bloki pasują do siebie bez kontaktu z metalem z możliwością niezawodnego połączenia galwanicznego poprzez elektrolit.
W tym przypadku płytki stykowe posiadają dodatkową kratkę i są oddzielone od siebie płytką oddzielającą.
Łączenie płyt w bloki zwiększa ich powierzchnię roboczą, zmniejsza całkowity opór całej konstrukcji oraz pozwala na zwiększenie mocy podłączonego obciążenia.
Na zewnątrz pudełka taka bateria posiada elementy pokazane na poniższym rysunku.
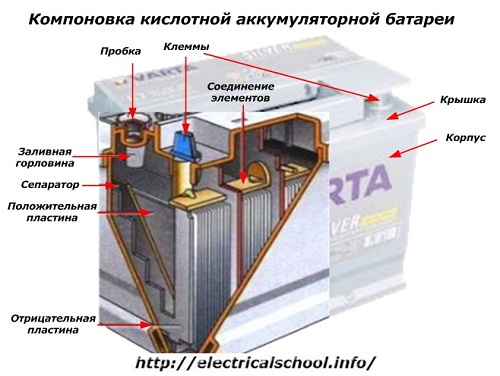
Pokazuje, że solidna plastikowa obudowa jest uszczelniona pokrywą i wyposażona w dwa zaciski (zwykle w kształcie stożka) na górze do podłączenia do obwodu elektrycznego samochodu. Oznaczenia biegunowości są wybite na ich zaciskach: „+” i „-”. Zwykle zacisk dodatni ma nieco większą średnicę niż zacisk ujemny, aby zapobiec błędom okablowania.
Nadające się do serwisowania akumulatory mają otwór wlewowy na górze każdego pojemnika, który umożliwia kontrolowanie poziomu elektrolitu lub dolewanie wody destylowanej podczas pracy. Wkręca się w nią zatyczkę, która zabezpiecza wewnętrzne wnęki obudowy przed zanieczyszczeniem i jednocześnie zapobiega wylaniu się elektrolitu przy przechylaniu akumulatora.
Ponieważ przy mocnym ładowaniu możliwe jest gazowanie z elektrolitu (a proces ten jest możliwy podczas intensywnej jazdy), w korkach wykonuje się otwory, aby zapobiec wzrostowi ciśnienia wewnątrz skrzynki.Tlen i wodór, a także opary elektrolitów wydostają się przez nie. Zaleca się unikanie takich sytuacji, w których występują nadmierne prądy ładowania.
Ten sam rysunek pokazuje połączenie elementów między rzędami i rozmieszczenie płytek elektrod.
Akumulatory samochodowe (kwasowo-ołowiowe) działają na zasadzie podwójnego zasiarczenia. Podczas rozładowywania/ładowania zachodzi na nich proces elektrochemiczny, któremu towarzyszy zmiana składu chemicznego masy czynnej elektrod wraz z uwalnianiem/absorpcją wody w elektrolicie (kwasie siarkowym).
Wyjaśnia to wzrost ciężaru właściwego elektrolitu podczas ładowania i spadek, gdy akumulator jest rozładowany. Innymi słowy, wartość gęstości pozwala ocenić stan elektryczny akumulatora. Do jego pomiaru służy specjalne urządzenie - areometr samochodowy.
Woda destylowana, która jest częścią elektrolitu akumulatorów kwasowych, zamienia się w stan stały - lód w ujemnych temperaturach.Dlatego, aby zapobiec zamarzaniu akumulatorów samochodowych w chłodne dni, należy zastosować specjalne środki przewidziane w przepisach do eksploatacji.
Jakie są rodzaje baterii?
Nowoczesna produkcja do różnych celów wytwarza ponad trzy tuziny produktów o różnym składzie elektrod i elektrolitu. 12 znanych modeli jest zasilanych wyłącznie litem.

Jako metal elektrody można znaleźć:
-
Ołów;
-
żelazo;
-
lit;
-
tytan;
-
kobalt;
-
kadm;
-
nikiel;
-
cynk;
-
srebro;
-
wanad;
-
aluminium
-
kilka innych przedmiotów.
Wpływają na charakterystykę mocy elektrycznej, a tym samym na zastosowanie.
Zdolność do wytrzymywania krótkotrwałych dużych obciążeń wynikających z obracania się wałów korbowych silników spalinowych przez rozruszniki elektryczne jest charakterystyczna dla akumulatorów kwasowo-ołowiowych. Znajdują szerokie zastosowanie w transporcie, zasilaczach bezprzerwowych i systemach zasilania awaryjnego.
Standard ogniwa galwaniczne (zwykłe baterie) są zwykle zastępowane bateriami niklowo-kadmowymi, niklowo-cynkowymi i niklowo-wodorkowymi.
Ale konstrukcje litowo-jonowe lub litowo-polimerowe działają niezawodnie w urządzeniach mobilnych i komputerowych, narzędziach budowlanych, a nawet pojazdach elektrycznych.
W zależności od rodzaju zastosowanego elektrolitu akumulatory są:
-
kwaśny
-
alkaliczny.
Istnieje klasyfikacja akumulatorów według przeznaczenia. Na przykład w nowoczesnych warunkach pojawiły się urządzenia służące do przesyłania energii — ładowania innych źródeł. Tak zwana bateria zewnętrzna pomaga właścicielom wielu urządzeń mobilnych w przypadku braku zmiennej sieci elektrycznej. Jest w stanie wielokrotnie ładować tablet, smartfon, telefon komórkowy.
Wszystkie te akumulatory mają tę samą zasadę działania i podobne urządzenie. Na przykład model palca litowo-jonowego pokazany na poniższym rysunku pod wieloma względami powtarza projekt akumulatorów kwasowych omówionych wcześniej.
Tutaj widzimy te same elektrody kontaktowe, płytki, separator i obudowę. Tylko one są wykonane z uwzględnieniem innych warunków pracy.
Podstawowe charakterystyki elektryczne baterii
Na pracę urządzenia mają wpływ parametry:
-
pojemność;
-
gęstość energii;
-
samorozładowanie;
-
reżim temperaturowy.
Pojemność nazywana jest maksymalnym ładunkiem akumulatora, który jest w stanie oddać podczas rozładowania do najniższego napięcia. Wyraża się ją w wisiorkach (układ SI) i amperogodzinach (jednostka pozasystemowa).
Rodzajem pojemności jest „pojemność energetyczna”, która określa energię uwalnianą podczas rozładowania do minimalnego dopuszczalnego napięcia. Jest mierzony w dżulach (SI) i watogodzinach (jednostki spoza układu SI).
Gęstość energii wyrażona jako stosunek ilości energii do masy lub objętości baterii.
Samorozładowanie uwzględnia utratę pojemności po naładowaniu przy braku obciążenia na zaciskach. Zależy to od konstrukcji i jest pogarszane przez awarie izolacji między elektrodami z wielu powodów.
Temperatura pracy wpływa na właściwości elektryczne iw przypadku poważnych odchyleń od normy określonej przez producenta może spowodować uszkodzenie akumulatora. Ciepło i zimno są niedopuszczalne, wpływają na przebieg reakcji chemicznych i ciśnienie otoczenia wewnątrz pudełka.
