Co to jest elektrolit
Substancje, w których prąd elektryczny powstaje w wyniku ruchu jonów, tj. przewodnictwo jonowenazywane są elektrolitami. Elektrolity należą do przewodników drugiego rodzaju, ponieważ prąd w nich jest związany z procesami chemicznymi, a nie tylko z ruchem elektronów, jak w metalach.
Cząsteczki tych substancji w roztworze są zdolne do dysocjacji elektrolitycznej, to znaczy rozkładają się po rozpuszczeniu na jony naładowane dodatnio (kationy) i naładowane ujemnie (aniony). W naturze można znaleźć elektrolity stałe, stopione jony i roztwory elektrolitów. W zależności od rodzaju rozpuszczalnika elektrolity dzielą się na wodne i niewodne oraz specjalny rodzaj - polielektrolity.
W zależności od rodzaju jonów, na które substancja rozkłada się po rozpuszczeniu w wodzie, elektrolity bez jonów H + i OH- (elektrolity solne), elektrolity z dużą ilością jonów H + (kwasy) i elektrolity z przewagą jonów OH- ( baza) można wyizolować.
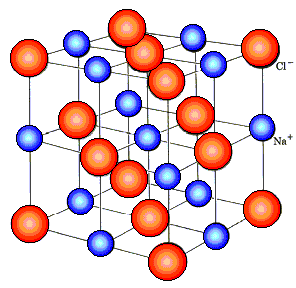
Jeśli podczas dysocjacji cząsteczek elektrolitu powstaje taka sama liczba jonów dodatnich i ujemnych, taki elektrolit nazywa się symetrycznym.Lub asymetryczny, jeśli liczba jonów dodatnich i ujemnych w roztworze nie jest taka sama. Przykłady elektrolitów symetrycznych - KCl - elektrolit 1,1-walentny i CaSO4 - elektrolit 2,2-walentny. Przedstawicielem elektrolitu asymetrycznego jest np. H2TAKA4 — elektrolit 1,2-walentny.

Wszystkie elektrolity można z grubsza podzielić na mocne i słabe, w zależności od ich zdolności do dysocjacji. Silne elektrolity w rozcieńczonych roztworach rozkładają się prawie całkowicie na jony. Należą do nich duża liczba soli nieorganicznych, niektóre kwasy i zasady w roztworach wodnych lub rozpuszczalniki o dużej sile dysocjacyjnej, takie jak alkohole, ketony czy amidy.
Słabe elektrolity rozkładają się tylko częściowo i znajdują się w dynamicznej równowadze z niezdysocjowanymi cząsteczkami. Należą do nich duża liczba kwasów organicznych, a także wiele zasad w rozpuszczalnikach.
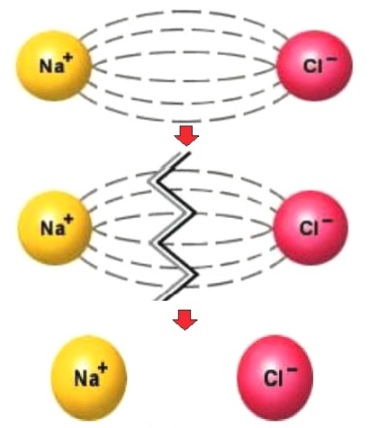
Stopień dysocjacji zależy od kilku czynników: temperatury, stężenia i rodzaju rozpuszczalnika. Tak więc ten sam elektrolit w różnych temperaturach lub w tej samej temperaturze, ale w różnych rozpuszczalnikach, ulegnie dysocjacji w różnym stopniu.
Ponieważ dysocjacja elektrolityczna z definicji generuje większą liczbę cząstek w roztworze, prowadzi to do znacznych różnic we właściwościach fizycznych roztworów elektrolitów i substancji różnego rodzaju: wzrasta ciśnienie osmotyczne, zmienia się temperatura zamarzania w zależności od czystości rozpuszczalnika i inni.
Jony elektrolitów często biorą udział w procesach elektrochemicznych i reakcjach chemicznych jako niezależne jednostki kinetyczne, niezależne od innych jonów obecnych w roztworze: na elektrodach zanurzonych w elektrolicie, podczas przepływu prądu przez elektrolit, zachodzą reakcje utleniania-redukcji, powstają produkty które są dodawane do składu elektrolitu.
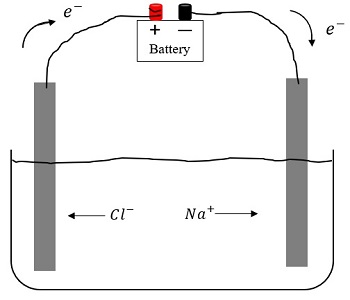
Tak więc elektrolity to złożone układy substancji, które obejmują jony, cząsteczki rozpuszczalnika, niezdysocjowane cząsteczki substancji rozpuszczonej, pary jonowe i większe związki. Dlatego o właściwościach elektrolitów decyduje szereg czynników: charakter oddziaływań jonowo-molekularnych i jonowo-jonowych, zmiany struktury rozpuszczalnika w obecności rozpuszczonych cząstek itp.
Jony i cząsteczki elektrolitów polarnych oddziałują ze sobą bardzo aktywnie, co prowadzi do powstawania struktur solwatacyjnych, których rola staje się coraz bardziej znacząca wraz ze zmniejszaniem się wielkości jonów i wzrostem ich wartościowości. Energia solwatacji jest miarą oddziaływania jonów elektrolitu z cząsteczkami rozpuszczalnika.
Elektrolity, w zależności od ich stężenia, to roztwory: rozcieńczone, przejściowe i stężone. Rozcieńczone roztwory mają strukturę podobną do czystego rozpuszczalnika, ale obecne jony zakłócają tę strukturę swoim wpływem. Takie słabe roztwory mocnych elektrolitów różnią się od roztworów idealnych właściwościami ze względu na oddziaływanie elektrostatyczne między jonami.
Przejściowy obszar stężenia charakteryzuje się znaczną zmianą struktury rozpuszczalnika pod wpływem jonów.Przy jeszcze wyższym stężeniu większość cząsteczek rozpuszczalnika uczestniczy w strukturach solwatacji z jonami, tworząc w ten sposób deficyt rozpuszczalnika.
Stężony roztwór ma budowę zbliżoną do stopu jonowego lub krystalicznego solwatu, charakteryzujący się wysokim uporządkowaniem i jednorodnością struktur jonowych. Te struktury jonowe wiążą się ze sobą iz cząsteczkami wody poprzez złożone interakcje.
Charakterystyczne dla elektrolitów są obszary ich właściwości o wysokiej i niskiej temperaturze oraz obszary o wysokim i normalnym ciśnieniu. Wraz ze wzrostem ciśnienia lub temperatury zmniejsza się uporządkowanie molowe rozpuszczalnika i słabnie wpływ efektów asocjacyjnych i solacyjnych na właściwości roztworu. A kiedy temperatura spada poniżej temperatury topnienia, niektóre elektrolity przechodzą w stan szklisty. Przykładem takiego elektrolitu jest wodny roztwór LiCl.
Dziś elektrolity odgrywają szczególnie ważną rolę w świecie technologii i biologii. W procesach biologicznych elektrolity służą jako medium do syntez nieorganicznych i organicznych, aw technologii jako podstawa produkcji elektrochemicznej.
Elektroliza, elektrokataliza, korozja metali, elektrokrystalizacja — zjawiska te zajmują ważne miejsce w wielu nowoczesnych gałęziach przemysłu, zwłaszcza w zakresie energetyki i ochrony środowiska.
Zobacz też: Produkcja wodoru metodą elektrolizy wody — technologia i urządzenia



